تبدأ رحلة من المختبر إلى الصيدلية في عالم تطوير الأدوية من داخل معامل البحث، حيث يتم تصميم الجزيئات دوائياً وتحليل بنيتها بدقة، ثم اختبار فعاليتها وسلامتها في مراحل متعددة قبل أن تصل أخيرًا إلى المريض في الصيدلية. في هذا المقال نستعرض هذه الرحلة العلمية خطوة بخطوة بلغة مبسطة وقابلة للفهم.
التصميم الجزيئي Molecular Drug Design
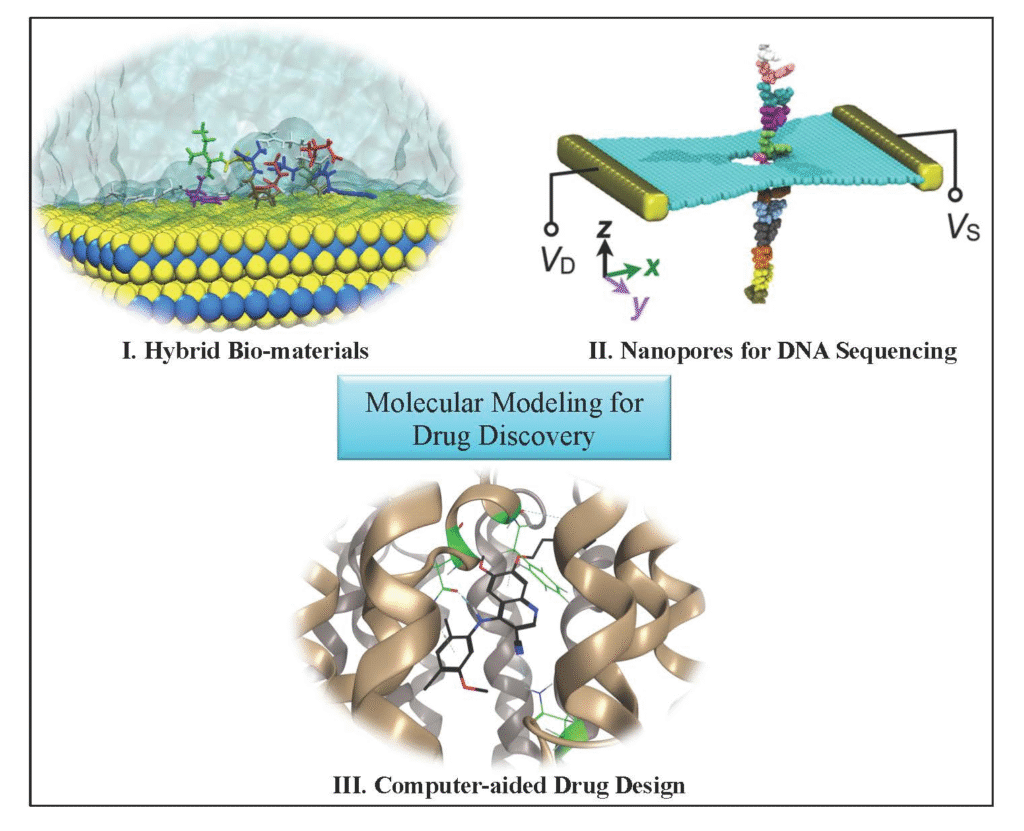
في هذه المرحلة، يقوم العلماء بتصميم جزيئات دوائية قادرة على الارتباط بمستقبلات داخل الجسم. ويعتمد ذلك على الكيمياء الحاسوبية وتقنيات مثل:
- Molecular Docking
- Molecular Modeling
- Structure-based Drug Design
- Ligand-based Design
هذه الأدوات تسمح بتوقع قدرة الجزيء على الارتباط بالهدف الحيوي، وعبور الأغشية الخلوية، وتقييم السمية المحتملة قبل إنتاجه فعلياً، مما يجعل رحلة تطوير الدواء أكثر كفاءة وأقل تكلفة.
التحليل الطيفي Spectroscopic Analysis — تأكيد البنية الجزيئية
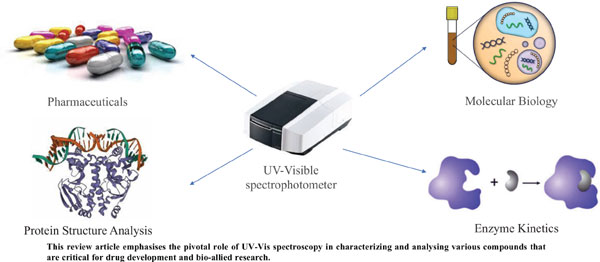
بعد تصنيع الجزيء تجريبياً، يجب التأكد أن تركيبه الكيميائي صحيح، ويحدث ذلك باستخدام عدة تقنيات تحليل طيفي أساسية في الكيمياء الدوائية:
NMR – الرنين المغناطيسي النووي
يحدد العلاقات بين الذرات داخل المركب ويكشف البنية الفراغية، مما يساعد على التأكد من أن الجزيء المنتج يطابق الجزيء المصمم نظرياً.
FTIR – التحليل بالأشعة تحت الحمراء
يكشف عن المجموعات الوظيفية Functional Groups مثل –OH و–NH2 و C=O، وبالتالي يؤكد وجود الروابط الكيميائية المتوقعة داخل المركب.
Mass Spectrometry – مطياف الكتلة
يحدد الكتلة الجزيئية ويكشف نمط التفتت Fragmentation Pattern، مما يساعد على تأكيد الصيغة الكيميائية ونقاء المركب الدوائي.
UV-Vis spectroscopy
يُستخدم لقياس تركيز المركب في المحلول، ويساعد في دراسة ثبات الدواء Degradation وسرعة تحلله تحت ظروف مختلفة.
هذه التقنيات تمنع انتقال مركبات غير صحيحة أو غير نقية إلى مراحل متقدمة من التطوير، وتُعد جزءًا جوهريًا في رحلة من المختبر إلى الصيدلية لأي دواء جديد.
التجارب الأولية Preclinical Trials — من الخلية إلى الحيوان
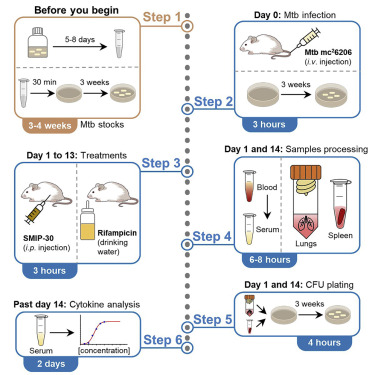
In-vitro — التجارب على الخلايا
يتم اختبار الدواء على خلايا داخل المختبر لتقييم:
- السمية الخلوية Cytotoxicity
- التركيز المثبط الفعال EC50
- الآلية البيولوجية للتأثير
تسمح هذه التجارب بفهم تأثير الدواء على مستوى الخلية قبل الانتقال إلى الكائن الحي الكامل.
In-vivo — التجارب على الحيوانات
تشمل اختبار الدواء داخل كائنات حية لتقييم:
- Pharmacokinetics — ADME (الامتصاص، التوزيع، الاستقلاب، الإطراح)
- Toxicity — السمية على المدى القصير والطويل
- LD50 — الجرعة القاتلة التقديرية
هذه المرحلة ضرورية لتقييم أمان الدواء قبل اختباره على البشر، وتُمثّل حلقة وسطية مهمة في سلسلة الانتقال من التركيب الكيميائي إلى الاستعمال السريري.
ملخص مراحل تطوير الدواء
| المرحلة | النشاط العلمي | الهدف |
|---|---|---|
| التصميم الجزيئي Molecular Drug Design | محاكاة ارتباط الجزيء بالمستقبل الحيوي | اختيار البنية الجزيئية المناسبة |
| التحليل الطيفي Spectroscopic Analysis | NMR، FTIR، Mass Spec، UV-Vis | التأكد من صحة البنية الكيميائية ونقاوة المركب |
| In-vitro | تجارب على خلايا داخل المختبر | اختبار السمية والتركيز الفعال EC50 |
| In-vivo | اختبار الدواء على الحيوانات | دراسة السمية والـ Pharmacokinetics |
| Clinical Trials | اختبار الدواء على البشر | إثبات الأمان والفعالية |
| Regulatory Approval | الحصول على الموافقات الصحية | تسويق الدواء وطرحه في الصيدليات |
يمكنك مراجعة المقالات التالي:
لمعرفة المزيد عن تقنيات الفصل والتحليل في الكيمياء التحليلية، يمكنك قراءة:
تقنية الكروماتوغرافيا في الكيمياء التحليلية
ولفهم أفضل للبنى الجزيئية الحيوية في الجسم، يمكنك قراءة:
من المختبر إلى الصيدلية .
تُظهر رحلة من المختبر إلى الصيدلية أن تطوير الدواء ليس خطوة واحدة، بل سلسلة مترابطة من التصميم الجزيئي الدقيق، والتحليل الطيفي المتقدم، والتجارب الخلوية والحيوانية، ثم الاختبارات السريرية على البشر، وصولاً إلى موافقات الجهات الرقابية. كل مرحلة تهدف إلى ضمان أن يصل للمريض دواء آمن وفعّال يعتمد على أسس علمية راسخة.